aido_plaido
в первом пункте третьей задачи неправильно посчитана энтальпия -3301,9 - (-3268) = -33,9 должно быть но там просто 33,9 и формула не правильная q=-h должно ведь быть не так ли ?
в первом пункте третьей задачи неправильно посчитана энтальпия -3301,9 - (-3268) = -33,9 должно быть но там просто 33,9 и формула не правильная q=-h должно ведь быть не так ли ?
Вы здесь отнимаете уравнение (2) от уравнения (1), у вас получится обратная реакция. Если путаетесь при работе с минусами можете попробовать поочередно: какую-то реакцию сначала “повернуть” в обратную сторону; получится обратная реакция с той же энтальпией, но с обратным знаком. Потом уже можно суммировать нужные реакции.
Зависит от того, как вы определяете q. Химики соглашаются теплоту обозначать положительной, если она повышает внутреннюю энергию системы, то есть когда система поглощает эту теплоту. В таком случае уравнение \Delta H = q верно (при постоянном давлении). Когда мы говорим не про термодинамические процессы, а про тепловые эффекты реакции, так уж сложилось, что за q мы обозначаем теплоту, которая выделяется, поэтому знак был бы противоположным.
Если вы просто написали q = \dots, вам вряд ли дадут балл, но если вы написали что-то наподобие “q кДж/моль теплоты выделяется”, можно апеллировать.
1 ответА все понял. Просто я пробежался глазами по ТеорМату и увидел формулу -h=q. Оказалась что не так( ну ладно. Капец я абоба.
В задаче сказано:
Известно, что К-селектрид – источник гидрид-аниона (такой как \ce{LiAlH4}), который в силу крупных втор-бутильных групп в данном синтезе восстанавливает несопряженные карбонильные группы в степени окисления +2.
Вы знаете механизм восстановления карбонильных групп с \ce{LiAlH4}?
1 ответИ так, для начала, чтобы понять это, следует сначала прочитать главу 17-4 McMurry 9th Edition.
"Известно, что К-селектрид – источник гидрид-аниона (такой как LiAlH4)… " – так написано в задании.
Восстановительные агенты бывают разными, например, как К-селектрид, самый распространенный это LiAlH4 (алюмогидрид лития). В LiAlH4 алюминий менее электроотрицателен, и связь Al-H в LiAlH4 более полярна: AlH4(-) + Li(+)
AlH4(-) – отрицательная частица из LiAlH4, хороший донор H(-), вернее отрицательного гидрид-иона.
У нас эту же роль, вернее роль донора гидрид-иона Н(-) играет К-селектрид. Почему? Потому что:
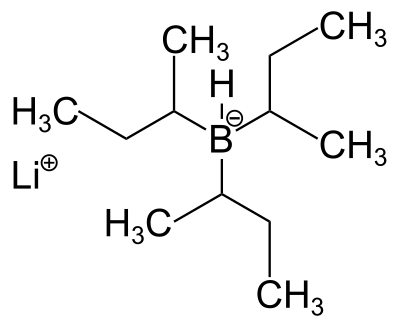
Здесь видно (представьте, что вместо лития калий), что водороду, присоединенному к отрицательному бору выгоднее “выйти” оттуда, откуда можно понять, что К-селектрид тоже предоставляет гидрид-ион. Это тоже восстановительный агент, но думаю и без картинки можно было понять из того, что там есть “водород”.
Этот отрицательный гидрид-анион – хороший нуклеофил. Он атакует именно тот угдерод, который больше всего электрофильный (не умею рисовать, прошу прощения, если не понятно) :
Это называется восстановление карбонильных соединений с помощью восстановительных агентов (LiAlH4, NABH4, селектриды K, Li и так далее, которые передают гидрид-анион).
1 ответспасибо:)
Есть очень старая книжка Роберт Касерио «Основы органической химии»
Раз на то пошло есть учебник английского языка))) Знание английского языка вас в жизни на световые годы вперед продвинет от незнающих.
Я когда начинал, без преувеличений каждое предложение по началу в переводчик пихал.
Я только 4 месяца назад писал Антону что не могу читать МакМурри, по этой же причине. Чтош, щас я на 12 главе)))
Все дело в том, что сопряженная карбонильная группа менее электрофильнее, чем обычная карбонильная группа. Это можно объяснить двумя способами :
Самый простой (и казалось бы, интуитивный) способ. Когда алкен сопряжен с карбонильной группой, он как бы делокализирует электронную плотность по всей сопряженной системе. А это значит, что карбонильный атом углерода тоже получает некую электронную плотность, что и делает его менее реактивным, чем несопряженная карбонильная группа
Когда ВЗМО (HOMO) алкена перекрывается с НСМО (LUMO) карбонильной группы, происходит стабилизация за счет образования двух новых ВЗМО и НСМО. Новая ВЗМО будет ниже по энергии за счет делокализации, а новая НСМО будет соответственно, выше по энергии, чем НСМО несопряженной карбонильной группы. Другими словами, когда нуклеофилу дают возможность проатаковать две разные электрофильные центры, он выберет тот центр, где НСМО будет ниже по энергии (в противном случае, перекрывание было бы не особо эффективным). Поэтому и нуклеофил предпочитает атаковать несопряженную карбонильную группу
Значит возможно?
Чтобы происходило восстановительное аминирование нужно что-то, что будет восстанавливать. Восстановителей в реагентах не было
На такие вопросы в органике почти всегда один ответ: да может. Почти всегда образуется смесь самых разных продуктов. Вопрос в том в каком количестве/соотношении.
В данном случае, @Madsoul объяснил почему енамин будет образовываться в другом положении.
Но я хотел бы заметить, что для решения этой задачи (и вообще, для решения задач по органике в целом) не обязательно понимать почему каждая реакция протекает так или иначе. Я полностью согласен, что это не самая очевидная вещь. Но из цепочки, из структуры интермедиата, становится понятно какая именно группа реагирует. И в этом искусство решения синтеза: не только пытаться понять “как именно будет реагировать” та или иная группа, а посмотреть на то, что будет дальше и попробовать понять что лучше подходит к последующим реакциям. Или посмотреть и заметить, что эта часть молекулы практически не меняется за 6 реакций, а значит, скорее всего она не реагирует. На худой конец - нарисовать оба варианта и проверить какой лучше подходит.
Возможность таких рассуждений в принципе и стала основной причиной почему я не добавил подсказку, что реагирует несопряженный карбонил.
1 ответХорошо, спасибо