Я понял как мы вывели это уравнение:
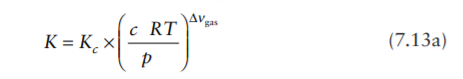
Но что мы сделали чтобы получить это:

???
Просто поделили газовую постоянную на давление, которое равно 1 бар (100 кПа). Тогда и получится что
Заметим, что \frac{8.314}{100} = 0.08314 = \frac{1}{12.027}
Стоп, а почему здесь килопаскали, а не паскали?
Паскаль используют когда объем берут в m^3(так как J=Pa\cdot m^3), в данном случае единицы измерения молярной концентрации \frac{mol}{L}, видно что они взяли объем в литрах, если объем в литрах то давление в килопаскалях
Спасибо.
Немного подробнее об этом. Удобно всегда использовать единицы измерения СИ — если все значения подставишь в СИ, можешь не волноваться о том, что у тебя получится на выходе — ответ будет в СИ.
Если взять значение R = 8.314, то мы сразу ставим конкретное ограничение — здесь R измеряется в \pu{Pa * m3 * K-1 * mol-1}. Что будет если в уравнение все подставлять в СИ?
Видно, что все сокращается и результат — безмерное значение. Но если мы захотим \pu{m3} в концентрации поменять на \pu{L}, получится следующее (единицы измерения по центру мы не можем поменять, потому что уже взяли значение 8.314 для R. Если поменяем единицы измерения, то поменяется и значение константы):
Значение уже не то, которое мы получали, подставляя все в СИ. Подставляя в \pu{mol m-3}, мы бы получили в 1000 раз меньшее значение, чем если бы мы подставляли в \pu{mol L-1}. (И получили бы уже не безмерную величину, а величину с измерением \pu{m3 L-1}) Чтобы скомпенсировать это изменение, можно поменять \pu{Pa} на \pu{kPa}.
То есть, мы не всегда можем такое проделать. В этом случае мы могли сделать так, потому что и объем и давление находились в знаменателе дроби. Если бы один из них находился в знаменателе, а другой — в числителе, такой фокус дал бы значение, в миллион раз отличающееся от того, которого мы бы получили, подставляя все в СИ.