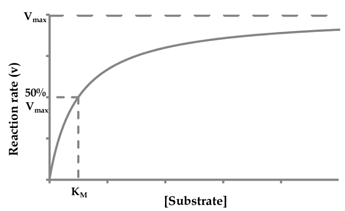
Объяснять график я начну с того, что предположу что ты знаешь что такое уравнение Михаэлиса-Ментен (но вот краткое напоминание):
Оно не очень удобно в плане построения графика и его оценки, поскольку график этого уравнения будет выглядеть как гипербола:
Для более удобной интерпретации графика и определения типов ингибирования используется обратное уравнение - все в -1 степени (double reciprocal plot):
График стал таким:
Он уже линейный - 1/[S] можно принять за x и тогда уравнение выглядит как y = ax + b. Тут же можно узнать точки пересечения графика с ОХ и ОY (на графике выше видно).
Далее что нужно знать, а точнее понимать, как различные типы ингибиторов влияют на Km и Vmax.
Есть три вида ингибиторов:
- Конкурентный(Competitive) - мимикрирует под субстрат и занимает активный сайт. Увеличивает Км.
- Смешанный(Mixed) - связывается с сайтом на ферменте отличным от активного, при этом может связаться как с ES так и с Е. Его частный случай это неконкурентный(noncompetitive) - он уменьшает Vmax.
- Бесконкурентный(Uncompetitive) - связывается только с ES комплексом на сайте отличном от активного. Уменьшает Vmax и увеличивает Км.
Смотрим на график в задании.
I. Тамифлю увеличивает Км - конкурентный ингибитор (уменьшается значение 1/Km)
II. Реленза - уменьшает Vmax (увеличивается 1/Vmax) - неконкурентный
III. Тамифлю конкурентный ингибитор - связывается с ферментом только когда активный сайт свободен
IV. Реленза неконкурентный ингибитор - связывается как с ферментом так и с ES комплеком.
V. В последнем дана скорость, но не дана концентрация субстрата и фермента, по графику без этого нельзя определить скорость.