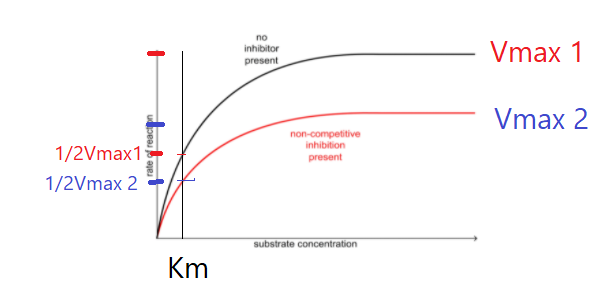
1)Как вообще выглядит реакция для бесконкурентных ингибиторов:

Теперь что такое Км:
K_{m}=\frac{k_{2}+k_{-1}}{k_{1}}
По сути Км обратно зависим от сродства фермента к субстрату. Мне кажется на эту проблему стоит смотреть со стороны химического равновесия. Поскольку ингибитор связывается с ES, концентрация ES уменьшается и равновесие реакции смещается в сторону образования ES - прямая реакция от E + S => ES ускоряется. Соответственно больше ферментов связывают субстрат.
2) Да здесь Vmax уменьшилсь и соответственно 1/2 Vmax тоже стала меньше, при этом чтобы достигнуть половины от максимума с ингибитором и без него требуется одинаковое количество субстрата.