Мне самому кажется, что они различаются растворителем. Если растворитель вода, то H3O(+), а если другой растворитель, то H(+)
Как пример, если взять аммиак в качестве растворителя, то Н(+) будет существовать в виде NH4(+).
Так они различаются?
Думаю ион водорода H+ будет слишком кислым и нестабильным чистом виде, и просто будет протонировать воду в растворе с огромным сдвигом в сторону продуктов реакции (H(+) + H2O = H3O(+)
И да, различаются, H+ просто пишут для упрощения в реакциях
Если не ошибаюсь, на одном из олимпиад Pagodane была задача,где рассматривали что на другой планете вместо H3O+ использывали NH4+,они все используются ради протонирование вещества, но исходный продукт может поменяться ,появиться nh2 связь ,зависит есть ли ещё реагенты кроме H3O+ или NH4+ .
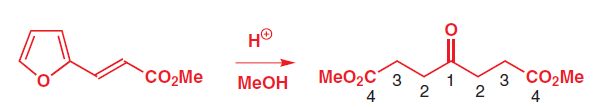
Просто в механизме этой реакции есть вода, а в реагентах не показали. Поэтому задался этим вопросом
В Клейдене во многих случаях сокращают так
В принципе, H^+ существует только в газовой фазе (подумай сам: это просто протон, это даже не атом). В любых растворах, H^+ будет связан с растворителем. Практически всегда, когда пишут H^+ на самом деле подразумевают именно H_3O^+, а H^+ пишут как сокращение
Ближе всего был @anxiety