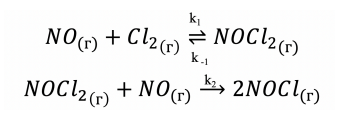
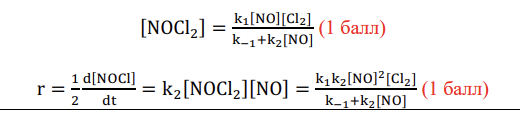
Облыс 2022 11 класс 3 задача
Формула я вывел почти правильно но не могу понять почему в конце не может быть еще умноженная на 2. Потому что по теормату d[NOCl]/dt=2k2[NOCl2][NO]
1 лайк
2 появится если мы захотим вывести скорость образование NOCl, что показано в уравнении ( d[NOCl]/dt умножено на 1/2). Скорость реакции подразумевает именно скорость успешного прохождения реакции. Давайте подумаем откуда появилась двойка? При столкновении реагентов образовалось 2 моль NOCl, но скорость реакции учитывает именно успешные столкновения, без учета того что образовалось именно 2 моль NOCl, поэтому в скорости реакции мы двойку не учитываем, но в изменении концентрации NOCl -учитываем
3 лайка
То есть мы еще учитываем 1/2 если нужно найти полное уравнение?
учитываем коэффицент если хотим найти скорость изменения концентрации реагента/ продукта от времени. Не учитываем коэффицент при нахождении скорости реакции
3 лайка
Все спасибо