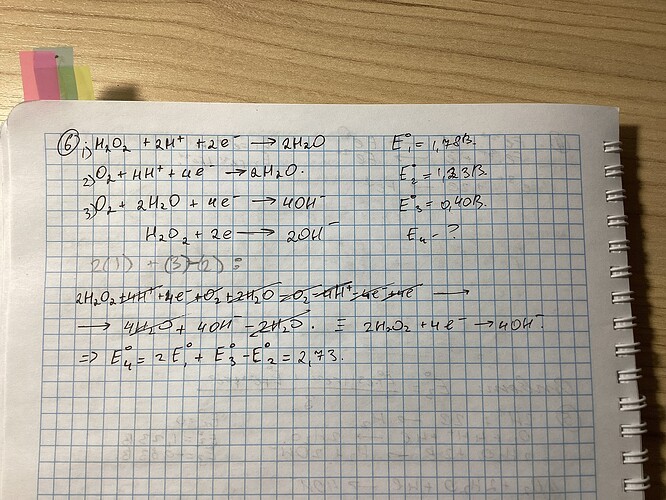не могу понять то, в чем ошибка
просто ответ выходит на 1,78 больше, чем надо
Даны стандартные окислительно-восстановительные по- тенциалы следующих процессов:
H2O2 + 2H++2e → 2H2O, O2 +4H+ +4e → 2H2O, O2 +2H2O+4e → 4OH−,
E◦ = 1,78 В, E◦ = 1,23 В, E◦ = 0,40 В.
Чему равен стандартный потенциал полуреакции
H2O2 + 2e → 2OH−?
Ответ. 0,95 В