The activation energy is the minimum energy needed for a reaction to take place upon proper collision of reactants. It is the definion of Ea in terms of kinetics.
Activation energy is the minimum quantity of energy which the reacting species must possess in order to undergo a specified reaction. Here is definiton in terms of energetics.
Для этой реакций ведь и вправду общая энергия активаций отрицательна, но как это можно представить?
Ну вот собственно тут и скрыт ответ
Типо когда E_1 + E_2 < E_3?
Даже если так, тяжело это как-то физический представить, типо отрицательная энергия, и какие выводы из этого можно сделать, типо реакция не будет идти, или наоборот слишком уж будет, раз уж так легко через барьер пройти.
Реакция просто будет замедляться при нагревании, понять и представить легко
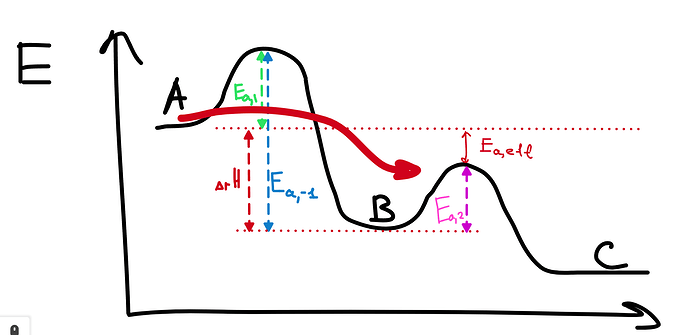
Если при этом первая реакция экзотермическая, и \Delta_r H + E_{a,2} \lt 0, то при нагревании у нас константа равновесия первой реакции будет быстрее уменьшаться, чем увеличиваться скорость второй стадии, отсюда и общее замедление
Я не понял как вы пришли к подобному выводу, типо то, что скорость второй реакций будет увеличиваться медленнее, чем уменьшаться константа равновесия первой.
Распишите через экспоненты произведение Kk_2
Типо так?:
Да, либо так
Видно, что при увеличении T, если E_{a,1}-E_{a,-1}<E_{a,2} то первые множители уменьшается быстрее, чем растет последний
Другими словами с увеличением температуры
e^{\frac{-\Delta H}{RT}} падает быстрее, чем растёт e^{\frac{-E_a2}{RT}}
Но как это можно понять вот так вот посмотрев?
Для наглядности можно взять производную или посмотреть что с логарифмом происходит в координатах 1/T
Но вообще развивайте математическую интуицию, и тогда это становится понятно с одного взгляда, например упражнения по рисованию графиков сложных функций неплохо развивают этот навык
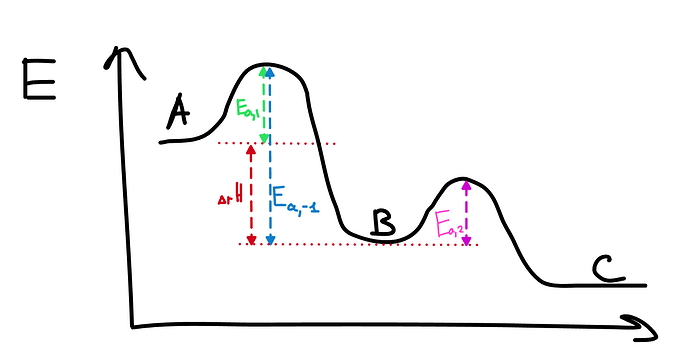
По итогу как таковой отрицательной энергией активаций нет, есть только отрицательная эффективная энергия активаций, которая описывается с помощью энергий активаций отдельных стадий, и эту эффективную энергию активаций мы не можем увидеть как таковой на графике, лишь можем судить с помощью неё как изменится скорость реакций с изменением температуры?
Ну как таковой нет, но на графике увидеть что-то подобное можно
В этом собственно смысл всех эти “эффективных величин”, слово “эффективный” буквально означает для нас “работает только для расчетов”
На графике ниже я что-то ее не вижу(эффективную энергию активации)