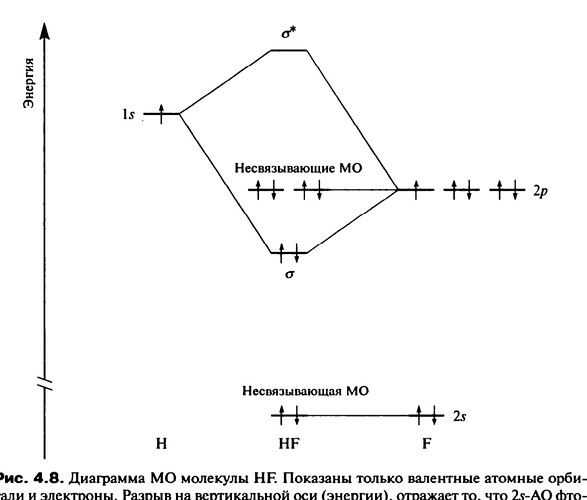
Почему у Водорода 1s орбиталь стоит выше по энергий чем 2p орбиталь Фтора и почему образуется несвязывающие МО? Помогите пж.
Чем выше электроотрицательность, тем ниже уровни энергии атомных орбиталей. Если сравнить электроотрицательности водорода и фтора, будет достаточно убедительно, что АО фтора ниже по энергии, чем АО водорода
Несвязывающие - значит не участвующие в образовании связи. Среди трех р-орбиталей только одна р-орбиталь может перекрываться с 1s орбиталью водорода с правильной симметрией. Две другие р-орбитали не могут перекрываться, так как перекрывание нивелируется разрыхлением. Собственно, поэтому две р-орбитали фтора являются несвязывающими
Как можно понять перекрывание нивелируется разрыхлением(они типо разрушаются?)
Можно еще один вопрос стоит ли пока изучать МО CO? просто кажеться это трудно понять.
Отменяется, если так можно выразиться
Хорошо спс
для чего?
МО молекулы СО не тривиальное, это да