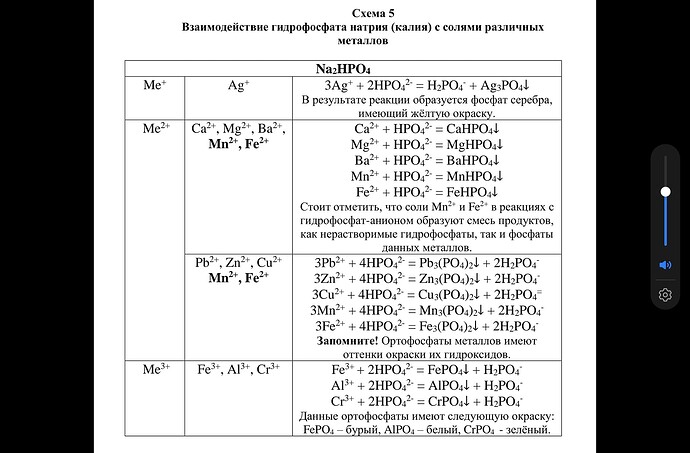
Здесь написано что ионы железа и марганца в растворе могут иметь две реакции и они образуют смесь нерастворимых продуктов гидрофосфаты и фосфаты.
3г но тут в реакции нитрата марганца с гидрофосфатом натрия образовывается только один осадок MnHPO4 и там написано что эта реакция более вероятна. Почему не идет образования осадка фосфата марганца и как понять какая реакция более вероятна?
Я не знаю точного ответа , но я предположил бы , что образование H2PO4- с Mn3(PO4)2 не так favourable как образования только одного осадка MnHPO4. Поэтому он и более вероятен. Если я ошибаюсь или другой ответ поправьте пожалуйста
Я сам не понимаю сильно. Но я думаю что мы это можем определить по доле ионов, оценив их просто примерно на глаз. Доли HPO4(-) H2(PO4)- PO4(3-) и так далее и у какого аниона выше доля с тем и выше вероятность образования ( конкретно тут они различаются скорее просто в зарядах и в количествах протонов, поэтому можно так утверждать думаю.)
В растворе Na2HPO4 скорее всего доля именно HPO4(2-) самая высокая. В целом примерные доли мы можем определять по кислотности среды. То есть в кислой среде преобладают формы с большими протонами, а в щелочной наоборот, меньшими. Тогда например при pH=12-13 у нас [PO4]3- больше всего, а при pH=2-4 [H3PO4] (примерно).
Иными словами надо смотреть конкретный pH когда речь идет о спорной ситуации что выпадает в осадок. Работает это только в случае сравнении таких сопряженных между собой анионов, с совсем разными анионами могут уже играть роль совсем другие факторы помимо pH.
Могу ошибиться, буду рад если исправите меня где то.
(P.S [PO4]3- вообще редко в реальных ситуациях есть в существенных количествах в растворе, так как чтобы он был в таких колиествах надо pH=12-13 судя по pKa.
Вообще, лучше всегда чекать Ksp и по ним считать