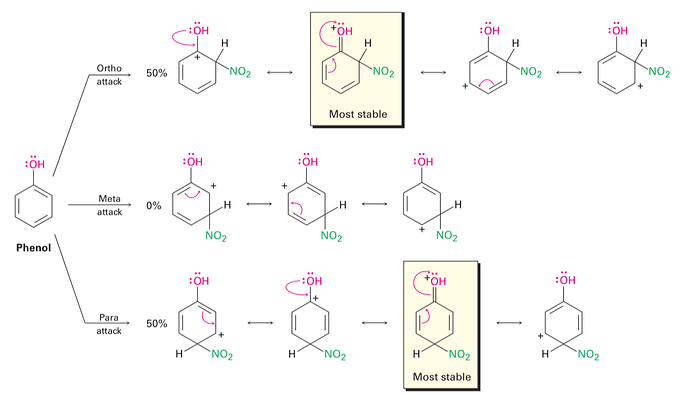
почему самая стабильная форма содержит положительный заряд на кислороде?
как они поняли что эти группы имеют более сильный электродонорный резонанс который перевешивает слабый электроотнимающий индуктивный эффект?
потому что кислород богат электронами, и положительный заряд на нем будет стабильнее чем на углеродах на которых и так мало электронов
он не слабый, просто слабее чем резонанс. Та структура с плюсом на кислороде вносит большой вклад, получается в реальной молекуле кислород несет частично положительный заряд, это перевешивает то, что он вообще стягивает электроны с соседних атомов и имеет частично отрицательный заряд
По моему из за того что, в этой резонансной структуре сопряженная система объёмнее( т.е кислород тоже sp2).
это не совсем правда. Как такой аргумент уживется с тем, что кислород электроотрицательнее углерода?
Здесь первостепенно то, что есть разница между карбокатионом с 6 электронами и катионом с 8 электронами (правило октета, туды суды).
В резонансных структурах, где положительный заряд на углероде – в окружении углерода 6 электронов.
В резонансной структуре, где кислород донатит пару – у кислорода по прежнему 8 электронов, но у каждого углерода теперь тоже по 8.
Ну, вот вы сидите и говорите: чисто теоретически, понятно, что у этих функциональных групп ED resonance effect но EW inductive effect.
Если превалирует ED эффекты, то у нас будут образовываться орто-пара продукты. Если EW – мета.
Потом вы проводите эксперимент и замеряете отношение изомеров. И находите, что орто-пара больше, чем мета. Вот так вы и понимаете, что ED resonance превалирует над EW inductive.
Вопрос, который, наверное, интересует вас больше – почему резонансный эффект превалирует над индуктивным. Один из способов ответить: резонансный эффект влияет на электронную плотность по всей цепи сопряжения. Индуктивный влияет лишь на ближайшие связи.
Вот это хорошее замечание. Читать надо внимательнее: weak и weaker несут разный смысл.
ооо этот ответ я искал , спасибо
Это еще означает, что у них разное количество связей. В структуре с сопряжением на одну связь больше, при том же количестве атомов:
В левой верхней 6 \sigma (CC), 2 \pi(CC),5(CH) и т.д. в следующей ровно те же + \pi(CO)
т.е. буквально в сравнении двух резонансных структур одна имеет больше связей, а значит с вероятностью 90% устойчивее. Вот если бы они имели одинаковое количество одинаковых типов связей, там да, наверное пришлось бы ломать голову, какая структура больший вклад вносит, где больше резонанса, где больше зарядов на более сильных атомах и т.п.