Типо у СО2 sp гибридизация и 2 двойные связи как надо, а у SO2 не так, но почему?
Потому что у серы 6 валентных электрона из них 4 электрона образует 2 пи связь 6-4=2 электрона не образует но участвует в гибридизацию. Углерод имеет 4 валентных электрона все электроны образует 2 пи связь
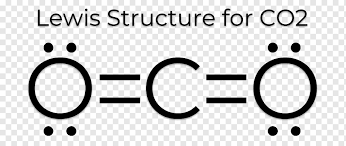
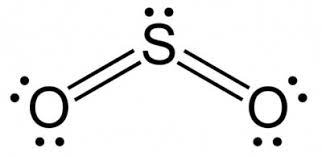
Немного нем понял, ведь для того, чтобы образовать 2 двойные связи нужно 2 p орбитали а у серы лишь одна и то она заполнена.
В теории валентных связей считается, что элементы третьего периода могут задействовать d-орбитали.
В теории молекулярных орбиталей это уже не так, и там SO2 и озон одинаковое электронное строение имеют, и имеют полуторные связи.
это же примерно из той же серии что и
И какая теория это объясняет? И как вообще элементы 3 периода образуют связи. (Башка не варит, нечего не понятно)
так ведь обе.
С точки зрения Теории Валентных Связей (ТВС), мы говорим, что у серы основная конфигурация 3s^2 3p^4 3d^0 , давайте наверное образуем 3s^1 3p^3 3d^2, получая гибридизацию sp^3d^2. Четыре электрона участвуют в образовании двух двойных связей, оставшиеся два сидят как НЭП.
Это полноценный ответ, который на этом этапе должен вас удовлетворить. Иными словами,
Можно часть электронов отдать на d-орбитали, и тогда все будет ок.
О чем говорит Илья, так это то, что если провести расчеты, окажется, что вклад d-орбиталей близок к нулю. Иными словами, “полу-практика” показывает, что аргументация ТВС не применима. И как же тогда можно объяснить? Тут на помощь приходит Теория Молекулярных Орбиталей (ТМО), которая говорит, что а нет никаких двойных связей, там связи полуторные, как в Озоне. Если вы не понимаете диаграммы, которые Илья прикладывал в ответе про тему “что-то не так с гибридизацией”, можете просто забить на ТМО пока не начнете изучать ее.