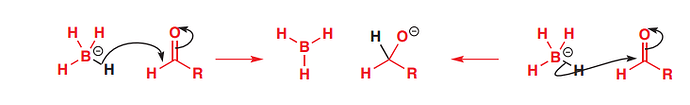
Мне не ясна разница между BH4- и H- заряженными частицами. Почему в реакции с карбонильной группой то, что гидрид-ион не способен вложить электроны в разрыхляющую пи орбиталь объясняется размером гидрид-иона, а NaBH4 способен это сделать? Ведь в BH4- также по факту протон с двумя электронами связывающей сигма молекулярной орбитали B-H идёт.
1 лайк
Очень жесткий и основный, предпочтет заняться чем-то другим
Ну это излишнее упрощение, так тогда любые кислоты и воду можно считать одинаково активными, ведь это просто протон на сигма связи.
Как например позабирать протоны вместо вкладывания электронной плотности в мягкую С=О разрыхляющую орбиталь?
Получается зависит от орбитали в которой находятся электроны нуклеофила? И аналогично электрофил зависит от того, какая именно орбиталь является вакантной?
1 лайк
Конечно. Нет одной шкалы нуклеофильности, разные нуклеофилы и электрофилы по разному склонны друг к другу. Общей теории нет, но закономерности интересные наблюдаются.
Жесткое-мягкое это самое грубое из них
2 лайка