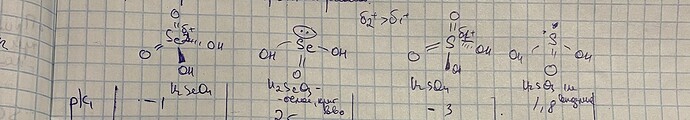
Немного не понимаю, почему селенистая кислота более устойчива чем селеновая ( потому что у селеновой есть два атома кислорода, которые сильно смещают электронную плотность на себя, тот факт что она более устойчива взят из разложения селеновой на селенистую), но при этом сернистая кислота менее устойчива чем серная, и вообще в свободном виде не выделена,хотя должен наблюдаться такой же эффект?
свойства элементов (и их соединений) разных периодов, даже если одинаковых групп , как правило, могут значительно отличаться ибо размер атома увеличивается, орбитали перекрываются хуже и т.д.(орбитали серы с кислодором перекрываются очевидно лучше чем селена)
если они перекрываются лучше, почему сернистая < селенистой по устойчивости
ну тут можно рассмотреть и продукты распада, скажем SO2 по той же причине стабильнее SeO2 (энтальпия формирования -297 кдж против -225), и наверное есть другие факторы, в итоге в сумме селенистая кислота будет чуть стабильнее
А при чем тут два атома, которые смещают плотность? Если вы рассуждаете не про кислотность, а про устойчивость, то вам нужно смотреть на энергетику связей, или реакций образования/разложения.
Попробуйте расписать энтальпию разложения из энергий связи и для серной и для селеновой.
Чтобы электроны были причиной образования ковалентной связи, они должны находиться в свободном доступе. Попробуйте рассмотреть электронную конфигурацию атомов серы и селена и отметьте разницу доступности s-электронов.
Подскажите пожалуйста справочные материалы чтобы найти энергию связи Se=O , S=O, поискала в интернете, там только связи по типу H-Cl, H-H , H-I . И вопрос, если я хочу сравнить термодинамическую устойчивость, то смотреть только на энергии связей. То есть ее нельзя объяснить электронным строением внешних атомов?
Для Se-O нашел только одинарную и то теоретическую оценку:
According to the Pauling equation, (30) estimated bond energies of Se–O and Se–S are 233 and 203 kJ/mol, respectively, and they are both lower than the bond energy of disulfide bond (240 kJ/mol) (источник)
Se=O найти не могу.
Возвращаясь к вашим вопросам.
Не обязательно. Достаточно вспомнить, что, например, при движении вниз по 4 группе постепенно наиболее стабильной становится степень окисления +2 (а для углерода она +4). Или вспомнить, что углерод образует удивительно стабильные C-C связи (благодаря чему мы с вами существуем), а кремний уже нет.
И это отчасти отвечает на этот вопрос. Вот как можно объяснить (с точки зрения простой модели атома) то, что углерод образует стабильные связи сам с собой, а кремний нет?
Я уверен (ну или хочется верить), что это можно объяснить если начать рассматривать квантовую модель атома, учитывать какие-нибудь релятивистские эффекты, спин-орбитальные взаимодействия и так далее. Но интуитивно объяснить это сложно.
Тут, наверное, тоже самое.
Назовите наиболее заметную разницу между серой и селеном с точки зрения электронного строения.