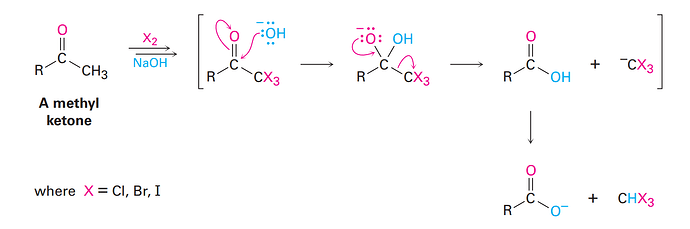
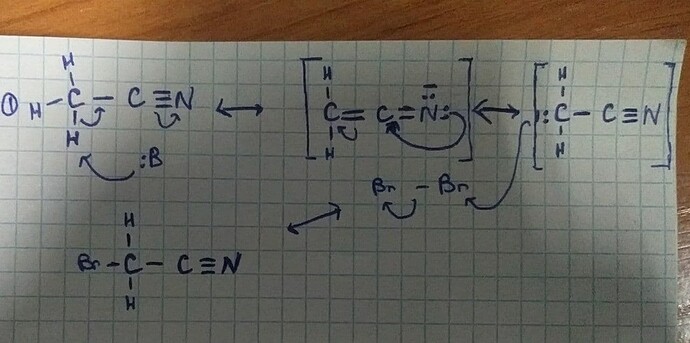
Почему эти реагенты плохо реагируют в реакции хлороформа?
реагенты:
\ce{H3CC\equiv N}, \ce{CH3CH2CHO}
Ну на счет альдегида можно подумать, что возможно уходящая группа не хорошая, \ce{H3CC^{-}Br2} . А других объяснении не придумал.
А что на счет ацетонитрила?
Общая реакция :
а что отличает нитрил от карбонила?
нитрил основнее карбонильной группы. То есть вы хотите сказать, что у ацетонитрила протоны не совсем кислые?
похоже на то. как это может мешать реакции?
Ну от слабой кислоты не может образовываться сильная кислота. Другими словами реакция будет более благополучной в сторону образовании реагентов
не понял. ты же помнишь механизм альфа-галогенирования? ответ кроется в нем(по крайней мере значительная его часть)
Ну я имел в виду, что ацетонитрил слабая кислота, а образующийся \ce{CHX3} кислота сильнее чем ацетонитрил. А мы знаем, из сильной кислоты должно образовываться слабая кислота. Но при этом у нас из сильного основание получается слабое, что тоже соответствует. Ну в этом плане я особо не думая написал
К сожалению прям ясного ответа не вижу пока что
самая первая стадия твоего механизма.
депротонирование нитрила. сравни рКа MeCN и MeCO. оцени, во сколько миллионов раз это депротонирование будет происходить