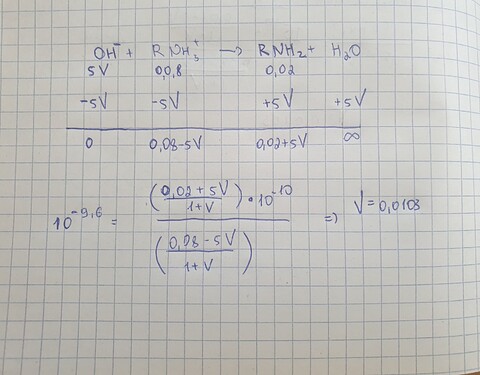У тебя есть мысли по решению задачи? Или ты не знаешь откуда начать?
Уравнение Хендерсона – Хассельбаха пригодится при решении пункта d, а чтобы решить пункт C нужно подумать, что вообще происходит в растворе при добавлении KOH.
KOH сильное основание, оно будет нейтрализовывать кислоту. В данной задаче есть единственная кислота - RNH3+ ( молекула, способная отдавать H+. )
Помимо этого, раствор у тебя немного разбавляется( начальные концентрации меняются), поэтому посчитаем моли каждой формы аминокислоты. Из пункта Б тебе уже известно, что 80% аминокислоты присутствуют в форме RNH3+, а остальное в RNH2. Вот решение на всякий случай
Дальше напишем уравнение реакции и таблицу, которая показывает изменение молей реагентов и продуктов. Объем добавленного KOH возьмем как V, тогда кол. вещества его будет 5V. Объем всего раствора увеличится до 1 + V. Использую константу кислотности нужно будет решить вот это уравнение.
( Чтобы упростить уравнение можно предположить, что объем сильно не изменится, тогда V в знаменателе пренебрегается. Ответ же это и подтверждает )