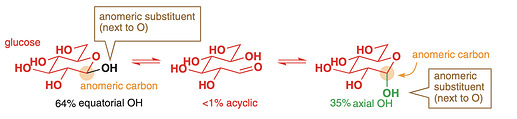
ну почему, он есть, аж 35% в аксиальной форме, без него вряд ли сильно больше пары процентов было бы.
Я так полагаю его вопрос почему с OAc аномерный эффект сильнее, чем с OMe.
Ответ, конечно же, в МО. аномерный эффект - простое смешение двух МО с образованием новых. НЭП кислорода лежат довольно низко по энергии. Все \sigma^* выше. Таким образом, аномерное взаимодействие имеет наибольший эффект когда \sigma^* ниже всего.
Что понижает энергию связи C-O? Однозначно ответить сложно.
На интуитивном уровне можно попробовать объяснить так: в результате аномерного взаимодействия, на -OR группе появляется частично отрицательный заряд (представьте экстремальную ситуацию когда происходит первая стадия Sn1/E1 реакции с образованием карбокатиона, который стабилизуется НЭП кислорода. Ну и получается, что чем лучше -OR группа стабилизирует отрицательный заряд, тем больше вклад этой «псевдорезонансной» структуры.
А MeO стабильнее, чем HO (метанол слегка кислее воды).
Другой, менее интуитивный ответ (хотя, скорее, предположение), такой. С одними и теми же атомами (по качественному составу), максимальный размах МО по энергии плюс минус одинаковый вне зависимости от количества атомов. Это, например, легко заметить в теории Хюккеля – низшая МО всегда \alpha + 2\beta, а высшая \alpha-2\beta. Конечно, в теории Хюккеля мы допускаем, что взаимодействуют только соседние атомы, что, конечно, неверно, но понятно что вклад 1,3 и 1,4 взаимодействий будет значительно слабее. Так вот, с увеличением сопряженной системы увеличивается кол-во орбиталей между этими двумя экстремумами. Так вот, может быть с увеличением размера группы (при движении от -OMe к -OAc) и при том, что новые атомы (речь про атом кислорода в C=O) соединены с предыдущими сопряженной системой, мы имеем тот же эффект? И может быть просто появляется новая LUMO орбиталь с каким-то вкладом C-O связи?