1 тур (Задачи)1 тур (Задачи)1 тур (Тапсырмалар)1 тур (Тапсырмалар)2 тур (Задачи)2 тур (Задачи)1 тур (Решения)1 тур (Решения)2 тур (Решения)2 тур (Решения)
Это обсуждение публикации https://olympiads.bc-pf.org/chemistry/national/2021/11
1 тур (Задачи)1 тур (Задачи)1 тур (Тапсырмалар)1 тур (Тапсырмалар)2 тур (Задачи)2 тур (Задачи)1 тур (Решения)1 тур (Решения)2 тур (Решения)2 тур (Решения)
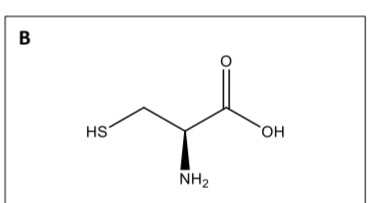
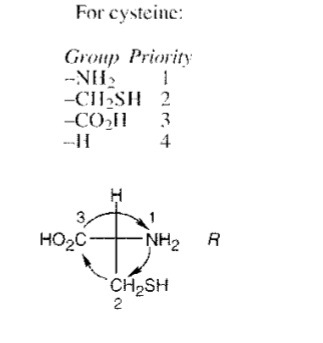
в задании сказано, что все аминокислоты в S конфигурации, разве для цистеина это не будет R конфигурацией?
Да, для L-цистеина будет R
Да, опечатка. Должны были сказать что у одного R конфигурация, а других двоих она S. Тогда, можно было бы на изи найти цистеин. Или возможно, что они в решении задачи вместо D-цистеина, L-цистеин случайно нарисовали
Идея с интегральным интенсивностями в том, что их сумма должна быть кратна/пропорциональна общему кол-во атомов водорода (посмотрите как решается предыдущий пункт).
Если повторить те же действия тут: (2+3.16+0.51)/7=0.81, т.е. соотношение протонов: 2.46:3.9:0.64 или 3.84:6:1. Получается сильно больше, чем кол-во протонов в C7H7NO. Задумка была следующая, ученик должен рассуждать так:
Дальше уже бензамид выходит довольно стремительно.
Откуда у вас уверенность, что ваше представление об индуктивной силе амида вернее спектра, который приведен в задаче? В задаче, к слову, экспериментальный спектр, не предсказанный теоретически. Т.е. if anything, ваши представления о силе групп должны обновляться с учетом этих данных, а не валидность спектра должна подвергаться сомнению.
Вообще, да, карбонильные группы оттягивают эл. плотность из кольца. Но, тут у нас не просто -COCH3 или COOH или COCl, у нас тут амид. А мы знаем, что вклад азота в карбонильную группу значительный (на этом построена стабильность амидной связи, а вместе с ней и всей жизни). Поэтому C=O группа не имеет такого же сильного воздействия на кольцо, как если бы азота там не было.
А то что пара протон поглощает в том же районе, что и мета – ну так вы посмотрите на спектр – там вполне возможно, что пики просто пересекаются и что там не идентичный сдвиг, а очень похожий. А вы даже не готовы поверить в то, что они похожи – опять же, индуктивный эффект ослабляется по мере отдаления от источника. 4 атома углерода это довольно далеко.
А почему их нельзя увидеть в том же хлороформе или других растворителях?
Значит в этом примере, мы должны были увидеть пик с интенсивностью 2, но из за того, что часть дейтерирована, и не видна на спектре, суммарная интенсивность оставшихся протонов показывается значение много ниже 2, однако это информация нам ничего не даёт о точном изначальном содержании протонов, поэтому приходится смотреть только на остальную часть спектра?
Значит тут мета углероды претерпевают только индуктивный эффект, и становятся деэкранированными только из за этого, а пара углероды чувствуют индуктивный эффект слабо, но зато мезомерный более-менее, и тоже деэкранируется, и по итогу их сдвиги должны быть схожи, а то что они идентичны просто совпадение?
Если бы они были прям-прям совсем идентичными, то мы бы не наблюдали мультиплет. То есть, это и есть следствие того, что несколько пиков сливаются почти в одном месте. Так как из-за слияния пиков визуально их не отделить, то принято их обозначать мультиплетом, что является характерным для колец.
У него есть сравнительно кислый атом D который может обменяться с кислым протоном в молекуле. pKa хлороформа 25, то есть сам он протон не отдаст, но в растворе всегда будут следовые количества D2O или других кислот/оснований, которые поспособствуют процессу.
Да
А разве как растворитель не используют чистый хлороформ?
Тогда он бы нифига ничего не отдал, имею ввиду протон. К тому же зачем эти соединения с дейтерием, типо почему используют тот же дейтерихлороформ, если их дейтерий мешает нормально проанализировать спектр? + что такое расширенный синглет
действительно
проблема в том, что 100% CDCl3 в природе не встречается. Вам нужно обогащать CHCl3. Надо ли объяснять, что добиться полного отсутствия CHCl3 крайне сложно?
потому что тогда сигнал, который вы снимаете в ЯМР спектрометре на 99.99% был бы вызван протонами CHCl3 просто потому что их в на несколько порядков больше?
Отсутствие протонов в растворителе как раз таки единственное, что позволяет анализировать спектр самого соединения. А то, что мы не видим кислые протоны – ну так это мелочь по сравнению с тем, что если бы сигналы всех протонов были неразличимы на фоне сигналов растворителя. И если мы хотим увидеть кислые протоны, мы всегда можем использовать ДМСО.