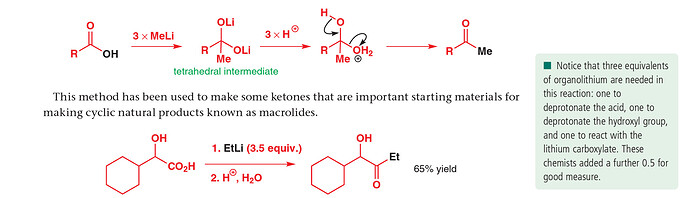
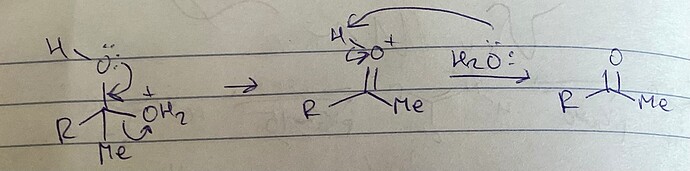
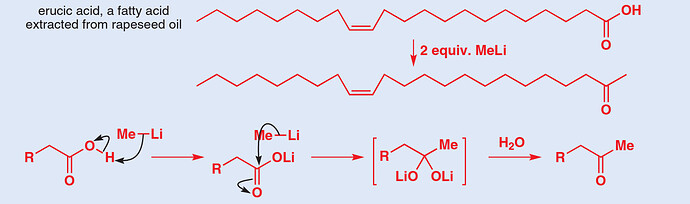
Не понял зачем добавлять третий MeLi. Первый пошёл на депротонирование кислоты. Второй пошёл на образование интермедиата. Все, дальше добавляем кислоту и получаем продукт. Есть предположение, что он для депротонирования О-Н в последней стадии (в книге так и сказано: для депротонирование ОН), но как он будет его депротонировать, если при добавлении кислоты, он сразу разрушится с образованием метана. Окей, тогда образуется соль лития, которая не будет точно депротонировать(если использовали, допустим, HCl). Но если подумать, что MeLi депротонирует воду, и образуется OH- который уже депротонирует тот ОН, то все ок. Но зачем добавлять MeLi, ведь вода тоже сможет депротонировать ОН:
Расскажу откуда это вообще вышло. Они хотели получить кетон из сл. эфира с помощью Гриньяра/литийорганики. Однако образовавшийся кетон был реактивнее чем исходный эфир, и получался только третичный спирт, вместо кетона.
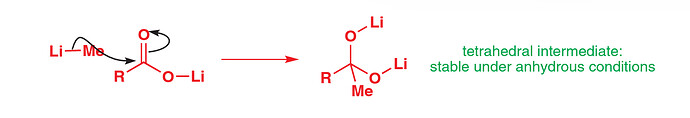
Чтобы решить проблему решили подобрать такое исх. вещество, которое давало бы продукт, который менее реактивен, чем оно само, чтобы гриньяр не реагировал с продуктом. Так и решили взять карбоксилат лития, который давал стабильный дианион с MeLi:
Мне кажется как раз таки метиллитий депротонирует воду, то есть 2 моля сначала идут на образование “дианиона”, потом уже у метиллития есть выбор откуда можно забрать протон, и так как pka у воды намного меньше чем у карбоксилата, и тем более дианиона, у нас получаются ионы OH- и метан, а на момент добавления кислоты в реакционной смеси уже нет метиллития, и соответственно оно не будет депротонироваться, может конечно быть такое что OH депротонирует кислоту, но там установится определенное равновесие, и все равно какое то количество OH будет доступно, которое потом и образует кетон
Откуда вода? До добавления кислоты все безводное же. На картинке сверху
stable under anhydrous conditions
Если воды нет, то ни у карбоксилата, ни у дианиона нет протонов для протонирования третьего MeLi.
Тогда может третий метиллитий добавляется после протонирования интермедиата кислотой, если кислота в малой концентрации и ее не останется после протонирования, тогдаметилитий точно может воздействовать на соединение, образовав кетон
Автор здесь ссылается на реакцию ниже, где в начальном соединении есть дополнительная гидроксо группа
Как подметил @Alibi, воды там быть не может, так что эту теория маловероятна.
А вообще все может быть намного проще: химик мог просто добавить избыток, чтобы реакция протекала полностью. Карбоксилат анион обладает самой высокой делокализацией, и поэтому может быть нереактивным даже к Гриньярду. Соответственно, чтобы сдвинуть равновесие и добавляется допольнительный эквивалент.
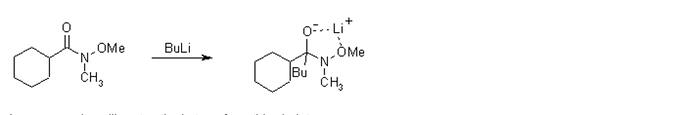
Бонусом здесь можно сказать еще о более популярной реакции Weinreb ketone synthesis. Опять же здесь при добавлении органометалики образуется относительно стабильный интермедиат, который дальше распадается при добавлении воды и повышении температуры. А засчет чего интермедиат при этой реакции стабилен понятно из рисунка.
Ждал пока кто-то скажет об этом). А как насчёт этого?
Тут гидроксила не видно, только R
Хотя может быть это и есть, но ведь чёрным по зелёному написано, что третий для гидроксила
я тоже думаю что там либо опечатка и должна быть двойка, либо они говорят о реакции ниже в более общем виде.