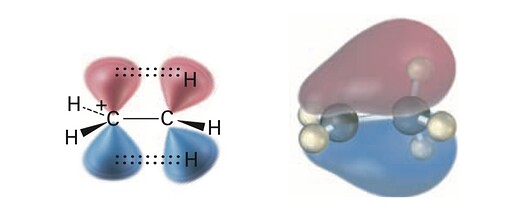
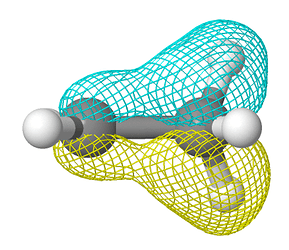
Размер тоже важен. Метильная группа лучше отдает электроны чем водород, так как 1) Метильная группа больше и 2) В метильной группе аж целых 3 электронной плотности б связи С-Н стягиваются.
(П.с. я не читал то что сверху. Возможно речь вообще не об этом)
Первая причина не фундаментальная (фундамент: стереоэлектроника). Она следствие второй причины.
Читайте секцию 7-9 в МакМури.
И какое же стабильнее?
правый карбокатион стабильнее. При определении стабильности карбокатиона играют два фактора: индуктивный эффект и гиперконьюгация. Они по силе примерно одинаковые. Точное взаимоотношение не скажу, но они достаточно похожи, чтобы суммарный эффект от этильной группы был сильнее эффекта метильной группы (при переходе от метила к этилу мы теряем одну гиперконьюгацию и добавляем одну более сильную индуктивную группу).
Более сильная индуктивная группа – это метил. Метил сильнее, чем Н-. Поэтому собственно при переходе от метильной группы к терт-бутильной у нас повышается стабильность карбокатиона.
Это же значит, что второе соединение стабильнее, т.к мы теряем гиперконьюгацию от 2 водородов, при этом получаем стабилизацию за счёт индуктивного эффекта 3 метильных групп.
Даже в этой формулировке я просто промолчу.
Но вообще, строго говоря, даже от -Me группы в гиперконьюгации участвует только одна С-Н связь.
Вы же сами сказали, что при переходе от метильной группы к тёрт-бутильной стабильность повышается, не значит ли это, что второе соединение стабильнее
Разве не 2?
Тьфу блин, это я уже поплыл и в голове у меня была картинка где неопентильный был слева. Да, совершенно верно, сейчас исправлю, прошу прощения.
Максимум одна связь в любой момент времени имеет правильную ориентацию
Что-то я тоже поплыл во всей этой орғанықе(пойду аниме смотреть что-ли) )
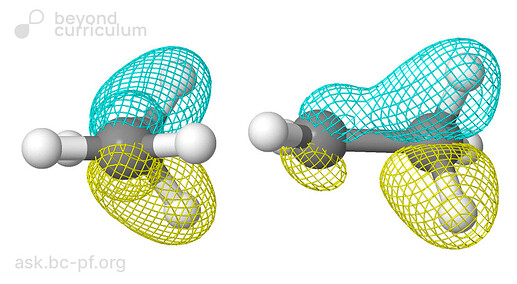
Вы про это? Тут же свободная орбиталь с двумя связями С-Н взаимодействует.
ахахахах угарнул с диалога чуток
А мне не нравится эта картинка))
А если серьезно. Я рассуждал так. Гиперконьюгация – это орбитальное взаимодействие, а орбитали лучше взаимодействуют когда они лучше перекрываются. Свободная р-орбиталь перпендикулярна плоскости катиона, значит (я предполагаю) лучше всего гиперконьюгация будет происходить когда есть С-Н связь которая коллинеарна этой орбитали.
А на картинке нарисован конформер 1, в котором две связи отклонены от р-орбитали на 60°. Вот его примерная геометрия (там один двугранный угол 55.9 другой 61.2, я не стал заморачиваться и пытаться найти идеальный угол):
C -3.768577 0.974915 -0.132447
H -2.904987 -0.457452 1.118718
H -4.247875 0.885867 -1.100266
H -4.070470 1.776793 0.531053
C -2.639357 0.073786 0.200529
H -2.424403 -0.666685 -0.574946
H -1.737056 0.663235 0.383737
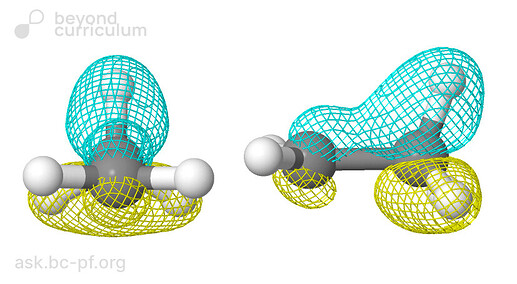
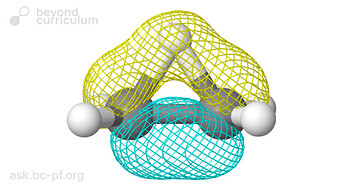
Гиперконьюгация выглядит примерно так:
У карбокатиона есть и такой конформер 2 (который я предполагал будет доминировать):
C -3.768577 0.974915 -0.132447
H -2.494553 0.009877 1.270687
H -4.247875 0.885867 -1.100266
H -4.070470 1.776793 0.531053
C -2.578949 0.148914 0.189303
H -2.663004 -0.836064 -0.278264
H -1.669765 0.634647 -0.174853
Примечательно, что если взять любой из конформеров и запустить оптимизацию геометрии (на уровне RI-MP2/aug-cc-pVTZ), они оба превращаются в изомер 3:
C -3.60353360561455 0.94435692921432 -0.13375317244204
H -2.38081265713507 -0.02673197463736 1.33335817078816
H -4.01536810319922 0.90143588357243 -1.13500894564053
H -3.83780180080417 1.79275876447010 0.49819375209501
C -2.79165172578453 -0.06971038013923 0.33164741229304
H -2.55873350328780 -0.91912276674098 -0.29940586086477
H -2.30529160417464 0.97196254426071 -0.28981835622886
А вот собственно энергии.
| Уровень теории | Конформер 1 | Конформер 2 | Изомер 3 |
|---|---|---|---|
| RI-MP2/(aug-cc-pVTZ/cc-pVTZ/C) | -78.650718612609 | -78.649519943654 | -78.670352906909 |
| MP2/aug-cc-pVQZ | -78.672911952904 | -78.671694711181 | -78.692978178902 |
Ну или относительные значения в \pu{kJ mol-1}:
| Уровень теории | Конформер 1 | Конформер 2 | Изомер 3 |
|---|---|---|---|
| RI-MP2/(aug-cc-pVTZ/cc-pVTZ/C) | 0 | 3.15 | -51.55 |
| MP2/aug-cc-pVQZ | 0 | 3.20 | -52.68 |
Иными словами, McMurry 1 : Антон 0.
раз уж проигрывать так с достоинством:
пару танцев с бубнами[1] и вот более-менее правильная геометрия
C 0.2884408845 -0.3272936457 -0.5667068831
H 1.3819965528 -0.3272936457 -0.5667068831
H -0.0632466576 -1.3624159873 -0.5667068831
C -0.3075742092 0.3514571016 0.6089238969
H -0.0551762935 0.1917851981 -1.4657778136
H 0.3448204508 0.7835275239 1.3572918208
H -1.3803940106 0.4264558930 0.7388256140
Ну и сразу вторая связь подключается в игру.
перевел в z-matrix, вручную изменил двугранные углы, перевел обратно в xyz ↩︎
\sigma(C-C) же тоже донатит эл-ны в р орбиталь, как σ(C-H), вроде не теряем же ничего
Это кстати можно по ямр понять. У толуола Ar-H водороды имеют более низкий пик, чем водороды бензола, соответственно, его кольцо богаче электронами чем бензол. То есть метил больше донатит чем водород
Я почему-то думаю, что делает она это менее эффективно, чем С-Н. Так ли это на самом деле — не знаю, не сильно вдавался в подробности.
Нашел хороший обзор, прочитаю как будет время.
P.S. А еще кто-то уже именно этил карбокатион изучал)) https://www.frontiersin.org/articles/10.3389/fchem.2013.00037/full