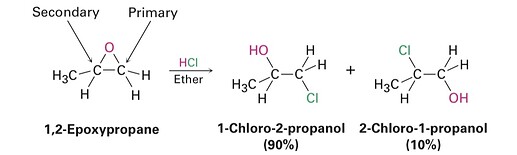
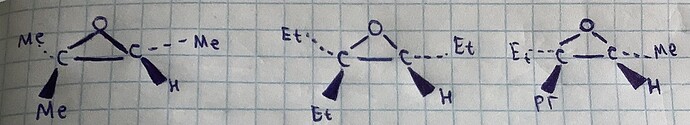
Почему когда это (кольцо) эпоксид, атака идёт на менее замещённую строну, если выбор между первичным и вторичным.
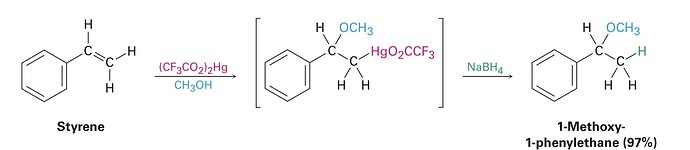
А когда это ртуть соединенный с 2 углеродами, то атака всегда проходит на более замещённую сторону?
Странное, на той теме вы ответили, что нулеофильное открытие кольца происходит по менее замещенной стороне, если там выбор между первичным и вторичным. Если же присутствует третичный углерод, то механизм будет похож на Sn1, и атака пройдёт по нему. Тут вроде все верно, как в книге.
Потом вы скинули это:
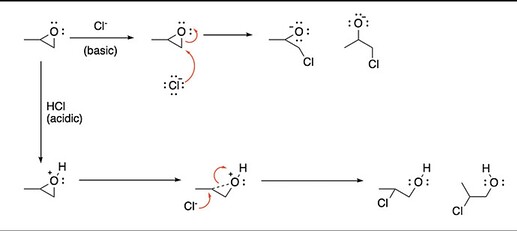
Тут видно, как при кислотном открытии кольца, появляется протонированный кислород, и так как вторичный углерод может его более менее стабилизировать, большая часть положительного заряда будет на нем, и атака пройдёт по нему.
Однако в книге же:
В книге же все немного по-другому, видимо они считают, что вторичный углерод не настолько крутой, что может нормально так стабилизировать положительный заряд, поэтому на нем конечно больше положительного заряда, чем на первичном, однако это не сопоставимо с тем, что на первичный напасть легче.
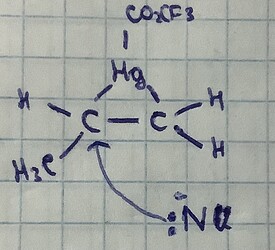
+ Я так и не понял, почему в случае с ртутью напасть на вторичный лучше, если судить по механизму из книги, то вторичный не намного больше стабилизирует заряд, чем первичный, но при этом на первичный напасть легче.
Я такое сказал?
Ну значит монозамещенный эпоксид даже в кислой среде раскрывается по менее замещенному положению. Картинку, которую я постил в той теме, я делал для иллюстрации влияния кислотности растворителя на региоселективность реакции. Т.е. да, правильней было бы нарисовать диметилоксиран, но в контексте той темы особо суть это не меняет.
В этом случае надо учитывать два фактора
- Насколько хорошо углерод стабилизирует положительный заряд
- Насколько хорошо этот положительный заряд стабилизирует кислород
Ибо от этого зависит как выглядит эпоксид: как слева или как справа.

Если как слева – атака будет идти по менее замещенному. Если как справа – по более замещенному.
Из примера с учебника можно сделать вывод, что положительный заряд на кислороде не хуже, чем положительный заряд на углероде.
Чем отличается трехчленное кольцо с ртутью?
P.S. У вас, к слову, структура соединения со с ртутью изображена неправильно (если это соединение, которое образуется в ходе традиционного оксимеркурирования)
Немного не понял, когда и куда атакует нуклеофил в кислой среде?
Хочу сказать, что примерно я понял, надеюсь подправите если ошибаюсь:
Есть два способа открытия эпоксидов:
- Кислотно-катализируемое открытие
- Основно-катализируемое открытие
В первом случае, сперва протонируется кислород, затем либо, этот положительный заряд по большей части стоит на нем, либо распределён по одному из углеродов, который может его стабилизировать, при этом он сам становиться более электрофильным.
Если же эпоксид образуют первичный и вторичный углероды, то заряд по большей части находится на кислороде, не с кем особенно не разделён, а значит никого более элетрофильным не делает, следовательно остаётся только напасть на один из углеродов, и открыть эпоксид, но сделать это легче всего напав на первичный углерод.
Ну а если мы имеем дело с третичным, и первичным или вторичным углеродами, то все немного иначе. Видимо, третичные углероды стабилизируют положительный заряд куда лучше, чем кислород, а значит этот заряд по большей части находится на третичном углероде, делая его более электрофильным, а если контентрация положительного заряда находится на нем, следовательно нуклеофилу ничего не остаётся кроме как напасть на него, не смотря на стерические затруднения.
Во втором случае никакого протонированного кислорода не образуется, все что есть, это обычный эпоксид, без вообще какого либо заряда. Не важно какие углероды входят в эпоксид, атака пройдёт по той части, куда легче всего напасть. Если первичный и вторичный, то на первичный, если третичный и вторичный, то на вторичный.
Мне кажется, что ртуть просто, по какой-то причине, стабилизирует положительный заряд хуже, чем третичные и вторичные углероды, а может даже чем первичные, поэтому почти всегда положительный заряд находится на более многозамещённом углероде, тот становится более электрофильным, и атака идёт по нему.
Уверены, а как правильно?
Я думал промежуточный продукт этой реакций именно такой
Я бы не стремился делать обобщенные выводы для всех первичных и вторичных углеродов. Что если заместитель у вторичного углерода -OMe или любая другая EDG?
Нам не обязательно делать такие радикальные выводы: куда лучше и по большей части. Достаточно чтобы одна из связей была бы слегка ослаблена (по сравнению с отсутствием этого эффекта), чтобы перенаправить региоселективность в ту или иную сторону.
Уверен.
С каким атомом связана ртуть вот на этой картинке
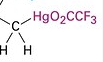
и на вашей?
Это ключ к разгадке.
А есть разница как именно он замещён?
Типо:
Вторичный есть вторичный, нету же разницы там -Me или -Et
Значит то, что я написал не верно? Если все было бы как я написал, то все было на своих полочках.
А почему именно связь R_{третичный} — О ослабевает?
С кислородом, значит моя ошибка была в том, что надо было написать кислород поближе к ртути?
Вы хотите сказать эти два карбокатиона имеют одинаковую стабильность?
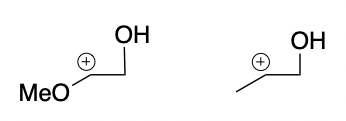
И да, даже в случае Me/Et есть разница. Более маленькая, но есть.
Ваша ошибка в том, что у вас ртуть связана с углеродом. Какой частичный заряд на ртути в этом случае? А какой если она связана с O-C(O)-CF3?
Разве когда мы говорим про первичный,вторичный,третичный мы не имеем ввиду коль-во связей, именно с углеродом? В вашем примере связь с кислородом
Да у него всегда частичный +
Ещё больший + наверное, т.к индуктивный эффект.
Когда речь идет про алканы – да. Но такая терминология применима/полезна в очень маленьком наборе случаев и поэтому иногда используют терминологию в смысле колечества углеродных групп.
Но хорошо, давайте сфокусируемся на вашем определении вторичного углерода.
Вы хотите сказать вот эти два карбокатиона имеют одинаковую стабильность?
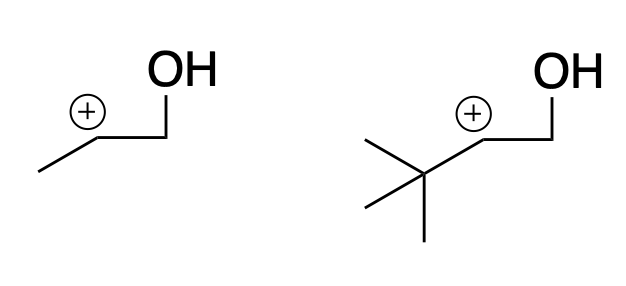
Хотите сказать, что если у меня есть метан, и я его превращю в метиловый спирт, он считается первичным?
То что показано на картинке думаю да, но жб там alkyl shift будет, и образуется третичный карбокатион, а это уже стабильно.
Не знаю кого вы и во что хотите превращать, из того что я сказал следует, что углерод в метиловом спирте можно назвать первичным если следовать “расширенной” терминологии.
Если я на респе или межнаре напишу, что углерод метилового спирта первичный, мне дадут баллы? И ещё, вы так и не сказали какой карбокатион более стабильный и почему.
у меня два ответа, выбирайте тот, который нравится больше:
- Сначала пройдите на респу/межнар, потом спрашивайте
- Какая, блин, разница?
Вы про это?
Если вы не можете ответить на этот вопрос – вам надо идти и перечитывать теорию.
А что касается изначального вопроса про ртуть, я задал достаточное количество наводящих вопросов, чтобы можно было сформулировать аргумент/объяснение.
Напоминаю:
Вам надо не просто ответить на эти вопросы, а еще понять почему я их вам задаю?[1] Почему ответы на эти вопросы важны для ответа на вопрос региоселективности?
Ответ на вопрос за вас формулировать я не буду.
я их задаю не потому что мне интересно узнать ваш ответ ↩︎
Обидно же будет потерять балл, в любом случае СН3-ОН, СН3-NH2, CH3-SH, все они первичные?
Я предполагаю, что второй карбокатион стабильнее, поскольку может произойти alkyl shift, и образоваться более стабильный третичный карбокатион. Гиперконъюкации кажется нету, вернее есть, но стабилизирует не так сильно, как в первом случае. Через индуктивный эффект кажется больше стабилизируется первое соединение. Тем не менее если случится шифт, а он скорее всего должен случится, то второе соединение все равно будет стабильнее.
В случае с ртутью постараюсь сформулировать аргумент:
Чем отличается трёхчленное кольцо с ртутью от эпоксидоного трехчленного кольца?
Ртуть помимо того, что соединен с двумя атомами углерода, соединен с кислородом, тем самым становясь \delta+ поляризованным.
Кислород в эпоксиде же, либо неитральный, либо полностью + заряженный.
И так, почему же нападение нуклеофила происходит с более замещённой стороны? Как по мне, причина в том, что этот самый \delta+ заряд по большей части распределен среди более замещённого углерода, и следовательно тот становится более электрофильным. По итогу мы имеем электрофильный атом углерода, на которого идёт нападение.
Потерять балл на чем? Как вы себе представляете задание, которое будет напрямую проверять этот аспект? Попросит вас сказать: каким является углерод в метиловом спирте?
Терминология это лишь инструмент общения, не более того. Мы используем терминологию “первичный/вторичный” для определенных целей, например для краткого обобщения неких результатов региоселективности. В S_N 2 реакции нуклеофил атакует по первичному углероду лучше, чем по вторичному, не потому, что один углерод первичный, а другой вторичный. Природа этого “предпочтения” (как и любого в органике) в стереоэлектронных факторах. Чтобы каждый раз не говорить “здесь есть влияние вот этого и вот этого, в сумме они дают это” мы кратко говорим “первичный vs вторичный” подразумевая более детальное объяснение.
Очевидно, что если один из заместителей связан не через атом углерода (как например OMe группа), это будет оказывать влияние на стереоэлектронику. Очевидно, что это будет влиять на региоселективность. Отражается ли это влияние в нашей обобщенной терминологии первичных/вторичных? Смотря какую именно терминологию использовать: узкую или расширенную.
На более практической ноте. Грубо говоря если вы скажете, что это соединение в основной среде раскрывается с одинаковой частотой слева и справа потому что оба углерода “первичные” (по кол-ву связанных углеродов), ваш ответ будет неправильным.

Еще раз. Первичность/вторичность это не фундаментальные правила химии. Это просто удобный способ коротко объяснить сумму стереоэлектронных факторов.
может. Но нужно ли нам его рассматривать в данном случае?[1]
Когда кажется креститься надо. Иными словами нет, неправильно.
учитывая то, что полноценный карбокатион НЕ образуется, мы лишь хотим узнать насколько положительный заряд был бы стабилизирован, если бы он образовался. Почему это важно? Потому что от этого влияет насколько сильно будет ослаблена связь с этим атомом углерода в протонированном эпоксиде (потому что чем сильнее она ослаблена, тем больше доля положительного заряда на атоме углерода. ↩︎
Спасибо, я понял почему даже если связь не с углеродом, мы можем назвать соединение первичным.
Почему нет?
В первом соединении карбокатионный углерод присоединён к метилу, он может немного так отжать электроны у углерода метальной группы, а тот эту потерю компенсирует тем, что ему 3 водорода тоже отдают свои электроны.
Во втором соединении карбокатионный углерод присоединен к tert-бутилу, он может отжать немного электронов у этого quaternary carbon, но тот не сильно так сможет эту потерю компенсировать, т.к метильные группы будут с меньшей охотой отдавать свои электроны.
Давайте сравним индуктивный эффект атома водорода (-Н) и метильной группы. Кто будет более сильным индуктивным донором?
Полагаю что -Н, менее электроотрицательный чем углерод ведь.