почему среднеквадратичная не равняется v^2 = ikT/m?
я знаю что находят через следующие формулы:
E=mv^2/v
E=ikT/2
тут i берут сразу за 3 равным, но это же справедливо лишь для одноатомной молекулы
почему среднеквадратичная не равняется v^2 = ikT/m?
я знаю что находят через следующие формулы:
E=mv^2/v
E=ikT/2
тут i берут сразу за 3 равным, но это же справедливо лишь для одноатомной молекулы
Но ведь в среднеквадратичную скорость лишь поступательные движения молекул добавляют. Как ты хочешь добавить вращение вокруг центра тяжести в поступательную скорость?
Дополню то, что сказал Илья:
Допустим энергия какой-то системы зависит квадратично от какой-то переменной х:
Чтобы найти среднюю энергию нужно воспользоваться формулой:
Функция распределения энергии выводится из распределения Больцмана и она выглядит так: (\beta=\frac{1}{kT})
Дальше если посчитать интеграл сверху выходит довольно простой ответ, который нам очень важен:
Из этого следует то, что вне зависимости от коэф. \psi и самой переменной x сред. энергия равна \frac{kT}{2}, но нужно учитывать что справедливо это только для энергий, которые квадратично зависят от определенного параметра.
Дальше уже все становится легко, найдем степени свободы различных атомов в разных состояниях:
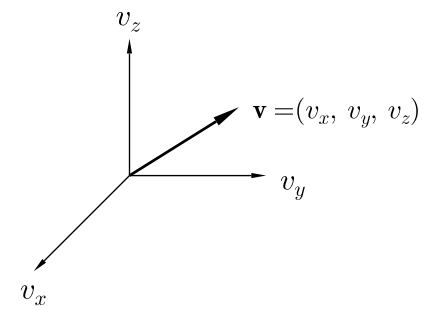
В одноатомном газе естественно может происходить только поступательное движение. Энергия и сред. энергия одного атома:
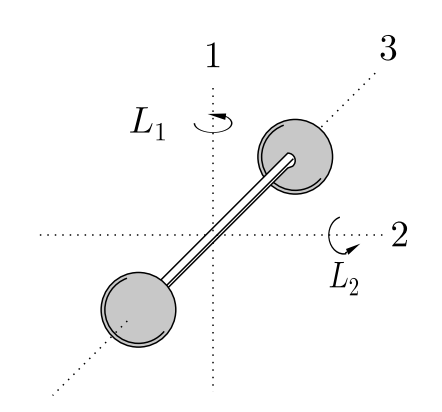
В двухатомном газе, в котором не происходит вибрационных движений могут происходить поступательные + вращательные движения (причем вращение происходит вокруг 2 осей). В этом случае энергия: (момент импульса: L=I\dot \theta)
Сред. энерг.:
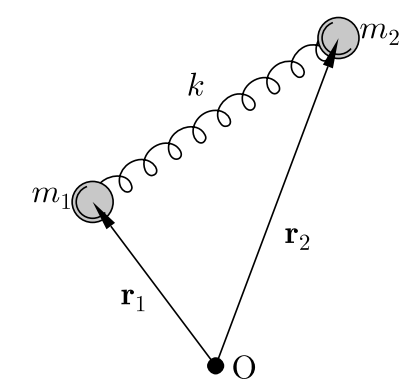
Здесь можно рассмотреть аналогичную систему из двух шаров, связанных пружиной
В этом случае энергия будет равна: (\mu =\frac{m_1m_2}{m_1+m_2})
Средняя энергия:
Думаю теперь должно быть понятно что в двухатомном и в других многоатомных газах степени свободы добавляются за счет вибрац. и вращ. движений
Ты знаешь, что такое степень свободы?
Степень свободы можно определить как число независимых координат, необходимых для однозначного задания положения системы. В таком случае изменение каждой из этих координат будет представлять собой некую скорость, которая добавляет составляющую в кинетическую энергию системы. Тогда так как на каждую такую составляющую, будет приходиться кинетическая энергия в виде kT/2 (в силу Теорема о равнораспределении — Википедия), то ты получишь соответствующее выражение для полной кинетической энергии молекулы.