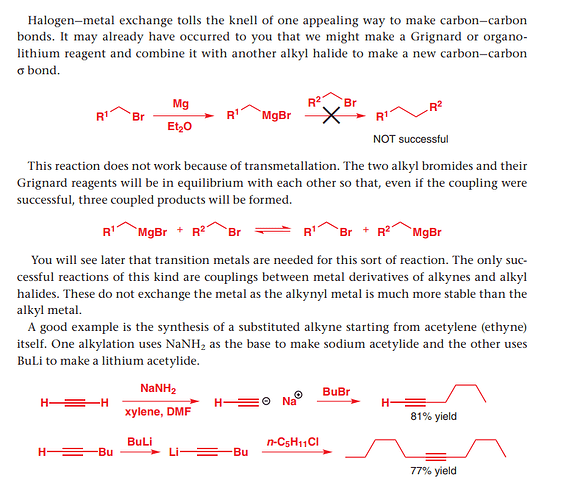
Здравствуйте. Как именно стабильности алкинила и алкила повлияли на то, идет ли эта реакция или нет? Алкинил ион намного стабильнее чем алкил ион, так как его свободная электронная пара делающая в алкиниле находится на sp орбитали, но у алкила на sp3. Этот момент мне понятен. Но как он именно имеет связь с тем, что реакция которая снизу происходит - я не понимаю.
Может так как делать transmetallation будет не выгодно, из за того, что стабильный алкинил анион и алкилбромид превращаются в алкинил бромид и не стабильный алкил анион, т.е вообщем это реакция не выгодна, и вместо неё идёт замещение. Но с другой стороны, почему не идёт элиминирование параллельно?
Вот скажем, есть у тебя две кислоты \ce{HA} и \ce{HB}, с константами диссоциации 10^{-5.32} и 10^{-9.21}, соответственно. Ниже приведены реакции диссоциации этих кислот:
Как ты думаешь, сможет ли основание \ce{B-} отщепить протон у \ce{HA}?
Сначала попробуй ответить качественно, а потом попробуй рассчитать константу равновесия вышеприведенной реакции.
Немного не понял, ведь о выгоде transmetallation ничего не говорится же?
Да, сможет. Кислоте же выгодно находиться в форме кислоты же, так как Константа диссоциации у него очень маленькая что означает очень большая часть вещества будет находиться в форме кислоты. В то же время кислота НА лучше диссоциирует на ионы чем первое, что означает ему выгоднее находиться в формах протона и сопряженного основания если сравнить ее с НВ, так?
я вообще не понял, что вы тут обсуждаете, и как это относится к первоначальному вопросу, но мне кажется вам стоит перечитать 12ю главу про кислоты и основания, если этот концепт до сих пор вызывает затруднения
но я еще не дошел до 12ой главы…
Да, совершенно верно.
Причина, почему @Madsoul привел в качестве аргумента значения pKa в том, что можно рассматривать pKa как некий показатель готовности основного центра формировать и удерживать хим связь. Логика такая: если В лучше держит протон, значит он будет лучше держать и металл. Поэтому зачастую значения pKa используются как прокси-метрика стабильности связей.
Я бы на этот вопрос отвечал по-другому.
Трансметаллирование
подразумевает разрыв связи \ce{R_1-Mg} и образование \ce{R_2-Mg}. Если эти две связи имеют схожие энергии, изменение энтальпии будет минимальным, изменение энергии Гиббса будет близко к нулю и реакция будет находиться в равновесии, в котором обе стороны представлены в схожих количествах.
Если же одна связь значительно сильнее другой, металл будет предпочитать сидеть с тем, где связь сильнее.
Связь алкинила с металлом сильнее по двум причинам. Во-первых, sp орбиталь ниже по энергии, значит и конечная МО ниже по энергии. Во-вторых, у алкинила есть заполненные \pi обитали, которые в теории (хз, наверное стоит проверить) могут взаимодействовать с пустыми p орбиталями магния с образованием back-bonding (как то, что происходит в металл-карбонилах, правда там электроны идут от металла к лиганду. Ну или как в оксо-комплексах, там электроны идут от лиганда к металлу).
@eudaimon оцени наши ответы. Тебе есть что добавить?
Anton, ваш разбор ситуации весьма детальный и информативный. Вы правильно указали на важность сравнения энергий образующихся связей для оценки протекания реакции трансметаллирования. Ваше объяснение относительно стабильности алкинил-металл связей благодаря их электронной структуре и возможности образования обратной связи (back-bonding) также заслуживает внимания.
Теперь позвольте мне добавить некоторые соображения. При рассмотрении реакции трансметаллирования мы должны учитывать как термодинамические, так и кинетические факторы. Термодинамически, как вы верно отметили, если разница энергий связей \ce{R_1-Mg} и \ce{R_2-Mg} невелика, то можно ожидать установления равновесия. Однако кинетические факторы могут сильно повлиять на реакционную способность и избирательность. Например, стерические и электронные эффекты могут замедлять или ускорять образование или разрыв определенных связей.
Что касается \pi-связей алкинов и возможности обратной связи с металлом, это действительно может быть фактором, способствующим стабилизации комплекса. Но для точного утверждения о существовании такого взаимодействия необходимы экспериментальные или теоретические данные, которые подтвердят наличие back-bonding в данной системе.
Возвращаясь к начальному вопросу о стабильности алкинил- и алкил-анионов и их влиянии на протекание реакции, мы можем рассмотреть их как промежуточные частицы в рамках механизма реакции. В контексте трансметаллирования, стабильность промежуточных анионов может влиять на положение равновесия и, следовательно, на общую выходность реакции. Сильная стабилизация одного из анионов может делать обратную реакцию менее вероятной, что сместит равновесие в сторону продуктов.
Поэтому, рассматривая трансметаллирование, мы должны учитывать как стабильность промежуточных анионов, так и стабильность конечных продуктов, и как эти факторы влияют на равновесие и кинетику реакции.
я ж тебе говорил не надо рассуждать слишком абстрактно, ты говоришь “кинетические факторы могут сильно повлиять”, что верно в общем случае, но мы говорим про конкретный случай трансметаллирования алкилмагний бромидов и алкинилмагний бромидов. Насколько различны эти две реакции с точки зрения кинетики? Не надо словоблудить.
Прошу прощения за предыдущую обобщенность. Давайте углубимся в конкретные детали реакции трансметаллирования алкилмагний бромидов и алкинилмагний бромидов.
В случае алкилмагний бромидов, кинетические факторы могут включать в себя стерическое затруднение вокруг магниевого центра, особенно если алкильный остаток объемистый. Это может замедлить обмен на алкинильный лиганд из-за затрудненного доступа к металлу.
С другой стороны, алкинильные магний бромиды имеют линейное распределение электронной плотности вдоль связи C≡C и могут быть менее стерически затруднены, обеспечивая более легкое приближение к магниевому центру. Тем не менее, их способность к обратной связи может увеличить энергетический барьер для отрыва алкинильного лиганда, что замедляет реакцию трансметаллирования.
Таким образом, с точки зрения кинетики, можно предположить, что трансметаллирование с алкинилмагний бромидами может протекать более медленно, чем с алкилмагний бромидами, из-за возможного укрепления связи металл-лиганд обратной связью. Однако для окончательных выводов необходимо учитывать конкретные алкильные и алкинильные группы, участвующие в реакции, и их влияние на кинетику. Экспериментальные данные могут дать более точную информацию о различиях в скоростях этих реакций.
Вот видишь, ты начал мыслить детальнее и уже понял (подсознательно), что изначальный тезис был неправильным. Со стерической точки зрения трансметаллирование алкинильных комплексов должно протекать проще/быстрее. Единственная причина, почему она может быть медленнее - если у реакции слишком большая энергия активации. Т.е. мы опять вернулись в плоскость энергетики.
Ваше замечание о стерических и энергетических факторах важно для понимания кинетики трансметаллирования. В случае алкинилмагниевых соединений, хотя они могут быть менее стерически затруднены, их более сильная связь с металлом из-за обратной связи может действительно привести к более высокой энергии активации для трансметаллирования по сравнению с алкильными аналогами.
Таким образом, если мы рассмотрим реакцию трансметаллирования как двухэтапный процесс, в котором первым шагом является диссоциация исходного алкил- или алкинил-магниевого соединения, а вторым — ассоциация нового алкилированного или алкинилированного фрагмента, то для алкинилмагниевых соединений первый этап может быть замедлен из-за более высокой энергии активации разрыва связи металл-лиганд.
Важно также учесть, что хотя стерические факторы могут способствовать более быстрой ассоциации, они не всегда являются определяющими для общей скорости реакции. Энергетика процесса, включая прочность связи металл-лиганд и возможность обратной связи, может оказать более значительное влияние на кинетику.
Итак, чтобы определить, какой процесс протекает быстрее, нужно учесть и сравнить энергии активации для диссоциации алкильных и алкинильных магниевых комплексов, а также скорости их ассоциации с новым лигандом. Экспериментальные исследования этих параметров обеспечат точное понимание кинетики реакции трансметаллирования в данных системах.
Во во, как раз хотел понять почему первая реакция не идет
интересно, заставляет задумываться
аа, Санж, верно. Металл просто не захочет идти к алкилу потому связь с алкинилом сильнее чем с алкилом как сказал Антон и трансметалляция не будет происходить. Но я не понял, что за элиминирование?
Большое спасибо всем за ответы!
Типо реактив Гриньяра это же капец какое мощное основание, и мне кажется он бы мог спокойно вместо замещения брома, забрать водород и выплюнуть бром, образуя алкен.
Не совсем. Сила основания \ce{CH3-} сильно отличается от основных характеристик \ce{CH3-MgBr}. Поэтому депротонировать алканы реактив Гриньяра к счастью не может.